Besoin d'information ?
Contactez-nous
You are here
NTM Elite agar
Isolement sélectif de Mycobactéries Non-Tuberculeuses (MNT)
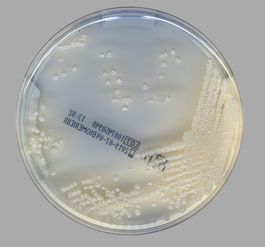
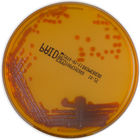
NTM Elite agar est un milieu sélectif innovant pour le dépistage et une aide au diagnostic par l’isolement de colonies de mycobactéries non tuberculeuses à partir d’échantillons respiratoires, y compris des échantillons de patients atteints de mucoviscidose
- Fertilité et sélectivité élevées
- Pas de phase de décontamination
- Utilisable en routine dans les laboratoires de microbiologie
Besoin d'information complémentaire ?
Largement présentes dans l’environnement, les Mycobactéries Non-Tuberculeuses (MNT) sont des pathogènes opportunistes qui peuvent causer des maladies pulmonaires chroniques. M.abscessus et le complexe M.avium sont les espèces les plus fréquemment rencontrées dans les infections pulmonaires. Associé à des lésions progressives des poumons, M.abscessus est également l’espèce de mycobactérie la plus résistante aux antibiotiques, extrêmement compliquée à traiter.(1)
Chez les patients atteints de Mucoviscidose, d’une Bronchopneumopathie Chronique Obstructive (BPCO) ou Bronchectasie, un diagnostic précis d’infection à MNT est essentiel afin d’aider les cliniciens à cibler le bon traitement et mettre en place les mesures appropriées.(2)
Conçue pour la culture sélective des MNT, la gélose NTM Elite agar est la version industrielle du milieu RGM. Elle permet un diagnostic plus facile et amélioré par rapport au milieu de culture AFB* couramment utilisé.
Amélioration du flux de travail et performances élevées
- Pas de décontamination préalable nécessaire
- Haute sélectivité : 85,6% versus 18,6%*
- Fertilité drastiquement améliorée : 95% versus 40%*
- Incubation à 30°C améliorant ainsi la croissance des MNT et inhibant la croissance des Mycobactéries du complexe Tuberculosis.
- Utilisable dans n’importe quel laboratoire de microbiologie
*Comparé à la méthode de référence AFB : Milieu Lowenstein Jensen associé au milieu MGIT
Lecture aisée

Isolement sélectif de Mycobactéries Non-Tuberculeuses (MNT)
(1) Pulmonary disease by non-tuberculous mycobacteria - clinical management, unmet needs and future perspectives.
Larsson, L. O., E. Polverino, W. Hoefsloot, L. R. Codecasa, R. Diel, S. G. Jenkins and M. R. Loebinger
Expert Rev Respir Med 2017 11(12): 977-989.
Lien PubMed : https://pubmed.ncbi.nlm.nih.gov/28967797/
Lien vers le site internet : https://www.tandfonline.com/doi/full/10.1080/17476348.2017.1386563
(2) US Cystic Fibrosis Foundation and European Cystic Fibrosis Society consensus recommendations for the management of non-tuberculous mycobacteria in individuals with cystic fibrosis.
Floto, R. A., K. N. Olivier, L. Saiman, C. L. Daley, J. L. Herrmann, J. A. Nick, P. G. Noone, D. Bilton, P. Corris, R. L. Gibson, S. E. Hempstead, K. Koetz, K. A. Sabadosa, I. Sermet-Gaudelus, A. R. Smyth, J. van Ingen, R. J. Wallace, K. L. Winthrop, B. C. Marshall and C. S. Haworth
Thorax 2016 71 Suppl 1: i1-22.
Lien PubMed : https://pubmed.ncbi.nlm.nih.gov/26666259/
Lien vers le site internet : https://thorax.bmj.com/content/71/Suppl_1/i1.long
| NTM Elite agar | ||
|---|---|---|
 |
Réf. 423144 | Coffret de 20 boîtes de 90 mm |
ARTICLES
- Stephenson D, et al. (Freeman Hospital). An evaluation of methods for the isolation of nontuberculous mycobacteria from patients with cystic fibrosis, bronchiectasis and patients assessed for lung transplantation. BMC Pulmonary Medicine (2019).
https://pubmed.ncbi.nlm.nih.gov/30665395/ - Brown-Elliott BA, et al. Evaluation of a novel rapidly-growing mycobacteria medium for isolation of Mycobacterium abscessus complex from respiratory specimens from patients with bronchiectasis. Heliyon, 2019.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6820269/ - Rotcheewaphan S, et al (NIH). Performance of RGM Medium for Isolation of Non Tuberculous Mycobacteria from Respiratory Specimens from Non-Cystic Fibrosis Patients. Journal of Clinical Microbiology. February 2019 Volume 57 Issue 2.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6355514/ - Scohy A, et al. Comparison of the RGM medium and the mycobacterial growth indicator tube automated system for isolation of non-tuberculous mycobacteria from sputum samples of cystic fibrosis in Belgium. J Clin Tuberc Other Mycobact Dis. 2018.
https://pubmed.ncbi.nlm.nih.gov/31720403/ - Plongla R, et al. (Chapel Hill NC). Evaluation of RGM Medium for Isolation of Non Tuberculous Mycobacteria from Respiratory Samples from Patients with Cystic Fibrosis in the United States. Journal of Clinical Microbiology. May 2017 Volume 55 Issue 5. 1469-1477.
https://pubmed.ncbi.nlm.nih.gov/28228494/ - Eltringham I, et al. Comparison of mycobacterial growth indicator tube with culture on RGM selective agar for detection of mycobacteria in sputum samples from patients with cystic fibrosis. Journal of Clinical Microbiology, 2016 August.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4963527/ - Preece CL, et al. (Freeman Hospital). Evaluation of Various Culture Media for Detection of Rapidly Growing Mycobacteria from Patients with Cystic Fibrosis. Journal of Clinical Microbiology. July 2016 Volume 54 Number 7. 1797-1803.
https://pubmed.ncbi.nlm.nih.gov/27098962/ - Preece CL, et al. (Freeman Hospital). A novel culture medium for isolation of rapidly-growing mycobacteria from the sputum of patients with cystic fibrosis. Journal of Cystic Fibrosis 15 (2016) 186-191.
https://pubmed.ncbi.nlm.nih.gov/26002312/
RÉSUMÉS ET POSTERS
ECCMID 2020
- Perry J, et al. Decontamination strategies used for AFB culture significantly reduce the viability of Mycobacterium abscessus in sputum samples from patients with cystic fibrosis.
Résumé # 2188. Session: Increasing knowledge on NTMs - PS022. Poster # P0517. - Vrignaud M, et al. Compatibility of the new NTM Elite agar with MALDI-TOF for direct isolation and identification of non-tuberculous mycobacteria.
Résumé # 2646. Session: Increasing knowledge on NTMs - PS022. Poster # P0511. - Vrignaud M, et al. Performances comparison between rapidly growing mycobacteria medium for direct-isolation of non-tuberculous mycobacteria, and its industrial version.
Résumé # 2047. Session: Increasing knowledge on NTMs - PS022- Poster # P0512. - Gafsi J et al. Performance of the NTM Elite agar for the detection of non-tuberculous mycobacteria in sputum samples of patients with cystic fibrosis.
Résumé # 5277. Session: Clinical challenges and culture-based diagnostics – PS104. Poster # P2407.
Le livre des résumés et posters 2020 de l'ESCMID est disponible gratuitement en format pdf sur le site de l'ESCMID.
Les résumés peuvent être trouvés avec leurs numéros.
ASM 2020
- Vrignaud M, et al. Appropriateness of Utilization of NTM Elite agar for the Diagnosis of Nontuberculous Mycobacteria Outside Biosafety Level 3 Laboratories.
Résumé # 4705.
Lire les instructions figurant sur l’étiquetage et/ou la notice d’utilisation du/des produit(s)
- Diagnostic Clinique
- Microbiologie Industrielle
- Services
- Actus & Évènements
- Documents
- À propos
- Ma sélection
bioMérieux France - 5, rue des Aqueducs - B.P 10 - 69290 Craponne - France
- Mentions légales
- Vie privée
- Cookies
- Plan du site
- Contact
- Copyright 2022 bioMérieux SA